
Abstrakt
Nyligen har Nanjing Liming Bio-Products Co., Ltd. (www.limingbio.com) SARS-COV-2 LGM/IgG Antikody Rapid Test Kit certifierats av det brasilianska National Health Supervision Bureau och erhållit ANVISA-certifieringen. Samtidigt listas också SARS-COV-2 RT-PCR och IgM/IgG-antikroppens snabba testpaket på den officiella rekommenderade upphandlingslistan över Indonesien. Under tiden, kalkande biostark®Novel Coronavirus (SARS-COV-2) multiplex PCR-kit i realtid, godkändes av Singapore Health Sciences Authority (HSA) och erhöll HSA-certifikatet.

Bild 1 Brasilien Anvisas certifiering
Brasilien (Anvisa) certifiering
Anvisas, känd som Agência Nacional de Vigilância Sanitária, är den brasilianska medicintekniska regulatorn. Det är nödvändigt att ett företag är registrerat hos ANVISA, National Health Supervision Agency, att sälja medicintekniska produkter lagligt i Brasilien. För att vara certifierad måste de medicinska apparater som kommer in i Brasilien uppfylla kraven från den brasilianska GMP tillsammans med de specifika standarder som de brasilianska myndigheterna har fastställt. I Brasilien klassificeras IVD -medicinska apparater i klass I, II, III och IV enligt risknivån från låg till hög. För klass I- och II -produkter används Cadastro -metoden, medan för klass III och IV -produkter används registreringsmetoden. Efter framgångsrik registrering kommer ett registreringsnummer att utfärdas av ANVISA, och uppgifterna kommer att laddas upp till den brasilianska databasen för medicintekniska produkter, detta nummer och dess motsvarande registreringsinformation kommer att visas på DU (Diário Oficial Da União).


Bild 2 Singapore Health Sciences Authority (HSA) certifikat


Bild 3 Den officiella rekommenderade upphandlingslistan över Indonesien

Bild 4 Strongstep®SARS-COV-2 IgM/IgG-antikropp RAPID-test
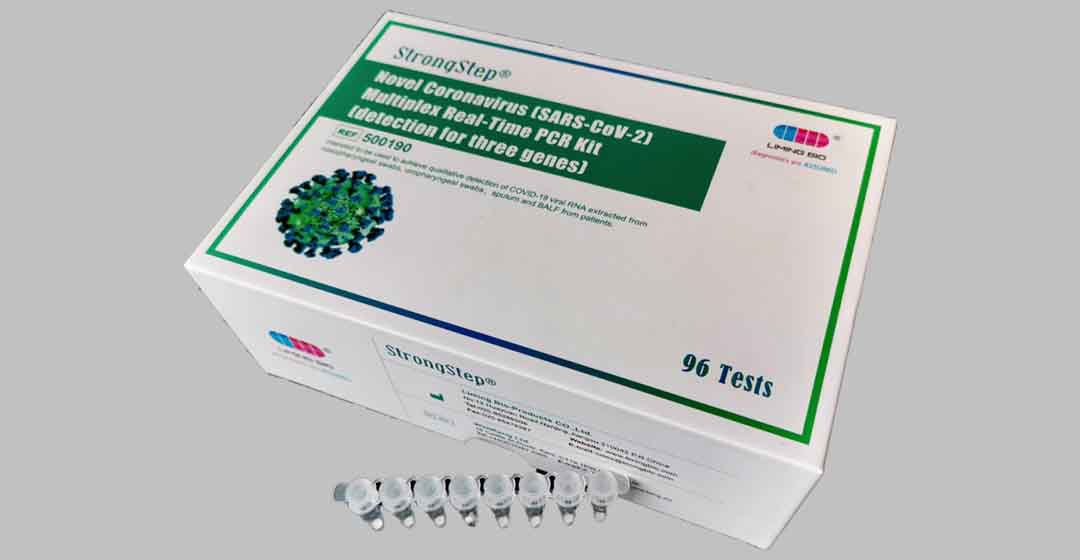
Bild 5 Novel Coronavirus (SARS-COV-2) Multiplex i realtid PCR-kit
Notera:
Detta mycket känsliga, färdiga PCR-kit finns i lyofiliserat format (frystorkningsprocess) för långvarig lagring. Satsen kan transporteras och förvaras vid rumstemperatur och är stabilt under ett år. Varje rör med premix innehåller alla reagens som behövs för PCR-amplifiering, inklusive omvänt-transkriptas, Taq-polymeras, primrar, sonder och DNTPS-substrat. Den behöver bara tillsätt 13ul destillerat vatten och 5ul extraherad RNA -mall, sedan kan den köras och förstärkas på PCR -instrumenten.
Svårigheten med kallkedjetransport av nya koronavirusnukleinsyrasdeagens
När konventionella reagens för nukleinsyrasetektering transporteras på lång avstånd förblir (-20 ± 5) ℃ Kylningskedjan lagring och transport för att säkerställa att bioaktivt av enzym i reagensen förblir aktiva. För att säkerställa att temperaturen når standarden behövs flera kilo torris för varje låda med nukleinsyratestreagens ännu mindre än 50 g, men det kan bara pågå i två eller tre dagar. I perspektivet av branschpraxis är den faktiska vikten av reagens som utfärdats av tillverkarna mindre än 10% (eller mycket mindre än detta värde) i behållaren. Det mesta av vikten kommer från torris, ispaket och skumlådor, så transportkostnaden är extremt hög.
I mars 2020 började covid-19 bryta ut i stor skala utomlands, och efterfrågan på nya koronavirusnukleinsyras detektionsreagens ökade dramatiskt. Trots de höga kostnaderna för att exportera reagensen i kallkedjan kan de flesta tillverkare fortfarande acceptera det på grund av den stora mängden och hög vinst.
Men med förbättringen av den nationella exportpolitiken för antipandemiska produkter, liksom uppgraderingen av nationell kontroll över flödet av människor och logistik, finns det förlängning och osäkerhet i transporttiden för reagens, vilket resulterade i framstående produktproblem orsakade genom transporten. Utökad transporttid (transporttid på ungefär en halv månad är mycket vanligt) leder till ofta produktfel när produkten når klienten. Detta har besvärat de flesta nukleinsyrarreagens exportföretag.
Lyofiliserad teknik för PCR -reagens hjälpte transporten av nya koronavirusnukleinsyradetekteringsreagens över hela världen
De lyofiliserade PCR -reagensen kan transporteras och lagras vid rumstemperatur, vilket inte bara kan minska transportkostnaden, utan också undvika kvalitetsproblem som orsakas av transportprocessen. Därför är lyofilisering av reagenset det bästa sättet att lösa problemet med exporttransport.
Lyofilisering innebär att frysa en lösning i ett fast tillstånd och sedan sublimat och separera vattenånga under vakuumtillstånd. Det torkade lösta ämnet förblir i behållaren med samma sammansättning och aktivitet. Jämfört med konventionella vätskreagens har de fullkomponenten lyofiliserade nya koronavirusnukleinsyrasetekteringsreagens som produceras genom kalkning av Bio följande egenskaper:
Extremt stark värmestabilitet: Det kan med stativbehandling vid 56 ℃ under 60 dagar, och reagensets morfologi och prestanda förblir oförändrad.
Normal temperaturlagring och transport: Inget behov av kallkedja, inget behov av att lagra vid låg temperatur innan du tappar ut, frigör helt kylförvaringsutrymmet.
Ready-to-användning: Lyofilisering av alla komponenter, inget behov av systemkonfiguration, undvik förlust av komponenter med hög viskositet såsom enzym.
Multiplexmål i ett rör: Detektionsmålet täcker nya koronavirus orf1Ab -gen, n gen, S -gen för att undvika virusgenovariation. För att minska falskt negativt används humant RNase P -gen som intern kontroll för att tillgodose det kliniska behovet av provkvalitetskontroll.
SARS-COV-2 IgM/IgG-antikropp Rapid Test och Novel Coronavirus (SARS-COV-2) Multiplex realtid PCR-kit (detektion för tre gener) har tidigare märkts i Storbritannien och nu accepterats och bearbetats av EUA av FDA i Amerika.
Nanjing Liming Bio-Products Co., Ltd. har alltid lagt kvaliteten på testpaketet i första hand och koncentrerar sig på utvidgningen av kapaciteten. Företaget kommer att tillhandahålla högkvalitativa testprodukter och tjänster av hög kvalitet till medicinska institutioner över hela världen och bidrar till den globala epidemiska förebyggande och kontrollen för att bygga en global gemenskap av delad framtid.
Long Press ~ skanna och följ oss
E-post:sales@limingbio.com
Webbplats: https://limingbio.com

Inlägg: JUL-06-2020







